Kontakt:Errol Zhou (Pan.)
Tel: plus 86-551-65523315
Mobil/WhatsApp: plus 86 17705606359
QQ:196299583
Skype:lucytoday@hotmail.com
E-mailem:sales@homesunshinepharma.com
Přidat:1002, Huanmao Budova, č.105, Mengcheng Silnice, Hefei Město, 230061, Čína
ViiV Healthcare je výzkum a vývoj léků proti HIV/AIDS řízená společnostmi GlaxoSmithKline (GSK) a Pfizer a Shionogi. Nedávno společnost oznámila, že Evropská agentura pro léčivé přípravky (EMA) Výbor pro humánní léčivé přípravky (CHMP) vydala pozitivní hodnocení naznačující schválení Rukobia (fostemsavir) 600mg tablet s trvalým uvolňováním, v kombinaci s jinými antiretrovirovými (ARV) léky , Pro léčbu multi-rezistentní HIV-1 dospělých, kteří nemohou postavit inhibiční antivirotikum.
Rukobia je nový inhibitor připojení k léčbě infekce HIV-1. V červnu tohoto roku, Rukobia byl schválen AMERICKO FDA pro indikace: v kombinaci s jinými léky ARV pro léčbu pacientů, kteří se snažili více HIV terapie (těžce léčba-zkušený, HTE) a jsou způsobeny rezistencí vůči lékům / nesnášenlivost nebo bezpečnost Zvažte multi-rezistentní HIV-1 dospělí, kteří selhali současný režim ARV. V pivotní studii BRIGHT fáze III byla většina (60 %) HTE multi-rezistentní HIV-1 dospělé infikované osoby obdržely Rukobia a optimalizovanou léčbu pozadí k dosažení a udržení virové suprese až do 96 týdnů, a CD4 + T buněčné technologie je klinicky k dispozici Význam zlepšení.
Významný pokrok v posledních několika desetiletích výrazně zlepšila léčbu HIV, a pro mnoho pacientů, HIV je považován za kontrolovatelné celoživotní onemocnění. Nicméně, vzhledem k rezistenci vůči lékům, snášenlivosti nebo bezpečnosti úvahy, dospělí pacienti hte (asi 6% HIV-infikovaných lidí) mají malou nebo žádnou možnost volby a jsou ohroženy progrese AIDS a úmrtí, a další možnosti léčby jsou naléhavě zapotřebí .
Schválení přípravku Rukobia na trhu poskytne důležitou možnost léčby pro osoby infikované multirezistentními HIV-1 dospělými viry HTE, kteří nemohou z různých důvodů užívat stávající léky k potlačení a udržení virové suprese. Dříve, AMERICKÁ FDA udělila Rukobia zrychlené kvalifikace, priority hodnocení kvalifikace, a průlom lék kvalifikace. Evropská unie EMA udělila Rukobia kvalifikaci pro zrychlené hodnocení.
Aktivní farmaceutickou složkou přípravku Rukobia je fostemsavir, což je prvotřídní inhibitor připojovacího systému HIV-1. Fostsavir je prodrug temsaviru. Po perorálním podání může být fostemsavir přeměněn na temsavir, který se pak vstřebává a má antivirové účinky přímým připojením k podjednotce glykoproteinu 120 (gp120) povrchu viru. Vazbou na toto místo na viru temsavir zabraňuje připojení viru HIV k CD4+ T buňkám hostitelského imunitního systému a dalším imunitním buňkám a zabraňuje infekci těchto buněk virem HIV a proliferování. Vzhledem k tomu, Rukobia je první antiretrovirová terapie pro první krok (připojení) viru cyklu, neprokázala rezistenci na jiné typy antiretrovirových léků, které mohou pomoci vyvinout rezistenci na většinu ostatních léků Drog-indukované infekce HIV.
Za posledních 30 let bylo dosaženo neuvěřitelného pokroku v léčbě HIV. Antiretrovirální léky mohou účinně inhibovat HIV, což pomáhá snižovat progresi onemocnění, přenos HIV a úmrtí související s AIDS. Nicméně, vzhledem k měnícím se schopnostem HIV, Někteří pacienti mohou vyvinout rezistenci na antiretrovirální léky, což má za následek jeho léčebný plán selhal. Problémy s snášenlivostí, bezpečností a lékovými interakcemi mohou dále snížit počet přijatelných antiretrovirových terapií při navrhování účinných možností léčby. Stále existují významné neuspokojené lékařské potřeby pro multi-rezistentní pacienti, kteří již dříve obdrželi více programů a nemůže úspěšně potlačit HIV. Výsledky výzkumu účinnosti a bezpečnosti z projektu klinického vývoje Rukobia ukazují, že lék má jedinečný potenciál pro multirezistentní pacienty infikované HIV, kteří potřebují nové možnosti léčby. Souhlas rukobie pro trh poskytne nový způsob, jak těmto pacientům pomoci dosáhnout virové suprese.
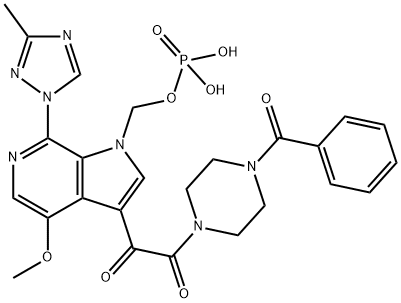
Molekulová struktura fostemsaviru
Pozitivní hodnocení výboru CHMP je založeno na údajích z pivotní studie FÁZE III BRIGHT (NCT02362503) u pacientů s HIV s více rezistentními léky HTE. Výsledky studie 96-week byly oznámeny na Mezinárodní konferenci AIDS Society AIDS Science Conference (IAS 2019) v Mexico City v červenci 2019.
BRIGHT je dvoutódová (randomizovaná a nenámánitizovaná) studie, která hodnotila bezpečnost a účinnost fostemsaviru inhibitoru připojizdu HIV-1 u dříve nadměrně léčených (HTE) dospělých infikovaných HIV-1. Do studie bylo zařazeno celkem 371 pacientů. Ačkoli tito pacienti užívali antiretrovirové léky (ARV), jejich hladiny viru v krvi (HIV-RNA) byly stále vysoké. Většina pacientů dostávala léčbu HIV po dobu delší než 15 let (71 %), podstoupila 5 nebo více různých způsobů léčby HIV (85 %) a/nebo měl v anamnéze AIDS (86 %) před vstupem do procesu.
Všichni pacienti zaznamenali rezistenci vůči lékům, nesnesitelnost a/nebo kontraindikace na 4 ze 6 aktuálně dostupných léků ARV. V randomizované kohortě (n= 272) musí pacienti udržovat plnou aktivitu na 1. Tito pacienti byli náhodně zařazeni v poměru 3:1 a slepě přibyli fostemsavir nebo placebo (n= 272) do svého současného neúspěšného léčebného plánu a dostávali funkční monoterapii po dobu 8 dnů. Pacienti (n=99), kteří neměli žádnou zbývající plnou aktivitu pro schválenou ARV, byli zařazeni do nenáhodné kohorty a v den 1 dostávali otevřený fostemsavir a optimalizovanou základní terapii (OBT). Primárním cílovým parametrem studie byla průměrná změna RNA HIV-1 v náhodné kohortě mezi 1. Po 8denním dvojitě zaslepeném období dostávali všichni pacienti v randomizované kohortě otevřený fostemsavir a optimalizovanou základní terapii. Mezi klíčové sekundární cílové parametry patří trvanlivost odpovědi po 24, 48 a 96 týdnech, jakož i změna bezpečnosti oproti výchozímu stavu v technologii CD4+ buněk a vznik virové rezistence.
Výsledky ukázaly, že na základě upraveného průměrného poklesu RNA HIV-1 od 1.<0.0001, intention-to-treat-exposure="" [itt-e]="" population).="" in="" a="" randomized="" cohort,="" the="" rates="" of="" virological="" suppression="" and="" immune="" response="" continued="" to="" increase="" from="" 24="" weeks="" to="" 96="" weeks="" in="" this="" difficult-to-treat="" multidrug="" resistant="" hiv-1="" patient="">
Specifické údaje: U pacientů léčených fostemsavirem a optimalizovanou základní léčbou (OBT) v randomizované kohortě byli ti, kteří dosáhli virologického suprese (HIV-1 RNA<40 copies/ml="" [c/ml])="" at="" 24,="" 48,="" and="" 96="" weeks="" of="" treatment="" the="" proportion="" of="" patients="" were="" 53%,="" 54%,="" and="" 60%="" (n="163/272)." with="" the="" passage="" of="" time,="" patients="" showed="" continuous="" immune="" improvement,="" and="" the="" average="" change="" of="" cd4+="" cell="" count="" continued="" to="" increase="" (90,="" 139,="" and="" 205="" cells/μl="" at="" 24,="" 48,="" and="" 96="" weeks="">
Ve studii, nejčastější nežádoucí účinky (≥5%, všechny stupně) byly nevolnost a průjem. V 96. týdnu byl podíl pacientů, kteří ukončili léčbu fostemsavirem kvůli nežádoucím účinkům, 7 % (randomizovaných: 5 %, nekatanitizovaných: 2 %).